California Üniversitesi’nde görevli bilim insanları corona virüsü salgınına sebep olan virüslerin nasıl davrandığına dair kritik bir araştırmaya imza attı… Bilim insanları, tahmin edilenden daha “sinsi” olan virüsün sağlıklı hücrelere ulaşmak için nasıl ilerlediğini keşfettiklerini duyurdu.
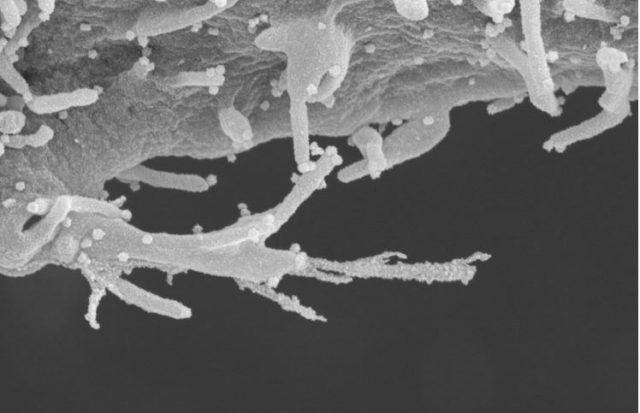
Sözcü: Üniversite bünyesinde çalışan bilim insanları mikroskobik görüntüleri kamuoyu ile paylaşarak, virüsün bulaştığı sağlıklı hücreyi dönüştürdüğünü gözler önüne serdi. Fotoğraflarda virüsün bulaştığı hücrelerden dokungaçlar (filopodia) çıktığı görülüyor. Uzmanlar, enfekte hücrenin bu dokungaçlar aracılığıyla yeni ve sağlıklı hücrelere ulaşamaya çalıştığını açıkladı.
Inside the body, the coronavirus is even more sinister than scientists had realized
Bu dokungaçlar aracılığıyla diğer hücrelere de virüs bulaştırıldığını açıklayan yetkililer, “Daha önce Covid-19’un sağlıklı bir hücreye tutunarak onu taklit ettiğini düşünüyorduk. Fakat bu keşif ile Covid-19’un aslında bir B Planı olduğu ortaya çıktı. Farklı şekillerde virüsü bulaştırabiliyor” dedi.
Araştırmayı yürüten Profesör Nevan Krogan, “Bu virüs o kadar sinsi ki hücreyi öldürmeden önce diğer hücreleri de enfekte edecek diğer mekanizmaları kullanıyor. HIV ve çiçek hastalığına sebep olan diğer hücreler de bu yöntemi kullanarak hastalığı yayıyor” dedi.
Bilim insanları Cell isimli tıp dergisinde yayınlanan araştırmanın, yeni tedavi yöntemleri bulmak için çok büyük bir önemi olduğunu da dile getirdi. Uzmanlar, “Bu filopodiaların büyümesini engelleyen 7 kanser ilacı var” dedi.
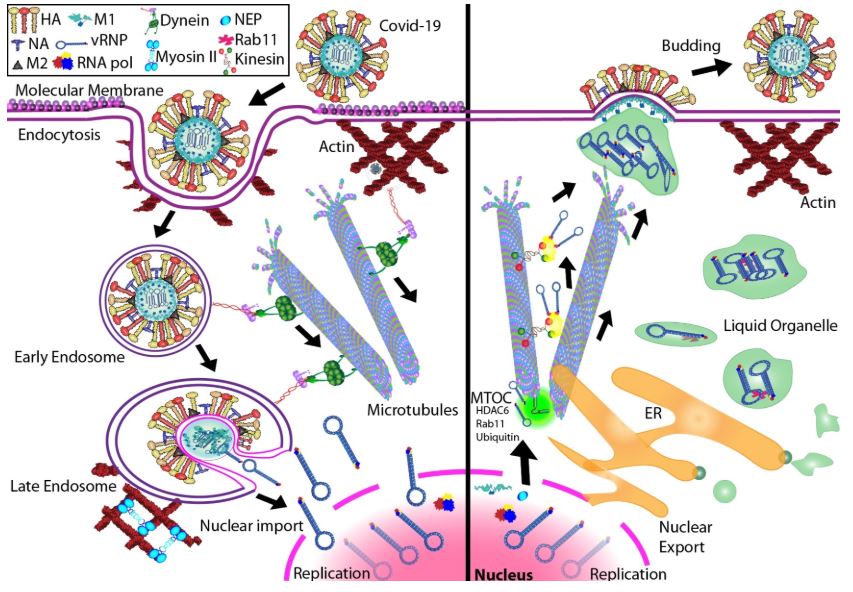
Coronaviridae için enfeksiyonun ilk aşaması, Spike (S) proteini yoluyla nöramidik asit gruplarına (dokuz karbon atomlu asidik karbonhidratlar) veya heparan sülfata Spike (S) protein aracılı bağlanmadır (3). Bu enfeksiyöz strateji çok etkilidir, çünkü bu docking moleküllerinin tüm memeli hücre yüzeylerinde birçok plazma zarı bağlanması için yüksek fazlalık yaratan türleri vardır. Bağlandıktan sonra virüs partikülleri, FAK / Cofilin / Rac / Cdc42 yolunu (4) düzenleyerek hücre iskeletini aktif olarak yeniden düzenler. Lv ve diğ. fare beyin nöronal (N2a) hücrelerine koronavirüs PHEV uygulandıktan sonra filopodia, lamellipodia ve stres lifi oranlarında geçici dalgalanmalar gösterdi. İlginç bir şekilde, 5 dakika içinde, stres lifleri büyük ölçüde tükendi, filopodia saptanabilir F-aktin içeriğine egemen oldu, toplam floresan phalloidin sinyalinin% 80’inin üretilmesi (4). 20-40 dakika arasında, lamelopodia eşit bir ortak oyuncu olarak ortaya çıktı ve son olarak 60 dakika sonra, oranlar normal seviyelere yakın bir seviyeye döndü, yani sinyalin% 60’ı stres lifleriydi. Bu makroskopik bir gözlem olmasına rağmen, nanometre ölçeğinde virionların kendi bireysel hücresel girişlerini düzenleyen yerel bir ortam oluşturabileceğini gösterir. Başka bir raporda, Owczarek ve ark. invajinasyon, vezikül eksizyonu ve F-aktin fonksiyonunu incelemek için koronavirüs OC43’ü insan kolorektal adenokarsinom (HCT-8) hücrelerine uyguladı (5). Klatrin bağımlı endositoz, kaveola bağımlı invajinasyon ve pinositozun tümü yedek viryon giriş mekanizmalarında yer almıştır. Vezik eksizyon ve giriş için büyük bir GTPaz olan dinamin gerekliydi (5). Viral girişin benzer çalışmaları Milewska ve ark. aktif endositoz veya viryonların diğer mekanizmalardan, örneğin kaveola bağımlı invajinasyon veya pinositozdan kitle etkili girişi ile, enfeksiyon oranı hücre yüzeyinin viral yüklenmesine bağlıdır (6). Hücresel giriş ayrıca virionu çekirdeğe yakın taşınan bir vezikülde paketler (5).