Kanser tedavileri tümör hücrelerini öldürmeyi amaçlar ve bağışıklık sistemi ortaya çıkan cesetlerden kurtulmakla görevlendirilir.
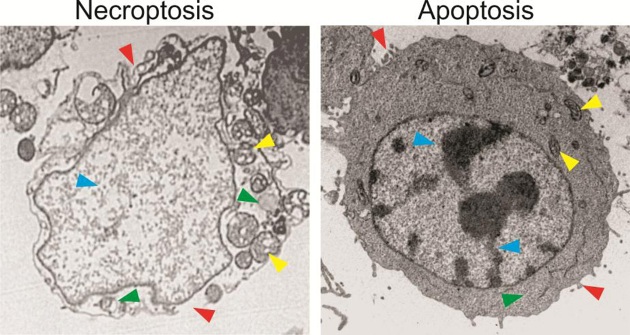
Kemoterapi gibi kanser tedavileri, tümör hücrelerini, örneğin apoptoz adı verilen bir süreçte onları kendi kendini yok etmeye, büzüşmeye ve sessizce ölmeye zorlayarak veya daha az yaygın olarak nekroptoz adı verilen daha patlayıcı bir hücre ölümü biçimini tetikleyerek öldürür.
Peki bu kanser hücrelerine öldürüldükten sonra ne olur?
Kanser hücreleri ölümle karşılaştığında, gereksiz veya hasarlı hücreleri vücuttan uzaklaştıran programlanmış hücre ölümü biçimi olan apoptozda olduğu gibi , zarları genellikle tehlikeye girer . Apoptozu tetikleyen moleküler anahtarlar “açık” konuma getirildiğinde, ölmekte olan hücre küçülür ve zarının bazı parçaları “kabarcıklar” halinde kırılır. Bu, hücrelerin iç bileşenlerinin dışarı sızmasına ve fagositleri veya hücresel kalıntıları sindirmekten sorumlu bağışıklık hücrelerini çekmesine neden olur.
Çağrılan fagositler, ölü kanser hücrelerini içine alır ve daha sonra onları, DNA’da bulunan zincir benzeri moleküller olan şekerler ve nükleik asitler gibi daha küçük bileşenlere ayırır. Bu işlem yoluyla ölü kanser hücreleri, diğer hücreler tarafından yeniden kullanılabilecek bileşenlere dönüştürülür .
Apoptoz durumunda (kanser tedavilerinin geleneksel teşvik etmek için tasarlandığı hücre ölümü türü ), hücresel bileşenler genellikle vücut tarafından atılmak yerine bu şekilde geri dönüştürülür.
Regulated Necrotic Cell Death in Alternative Tumor Therapeutic Strategies
Kanser tedavileri bazen hücrelerin küçülmek yerine şişip patladığı nekroptoz gibi diğer hücre ölümü türlerini de tetikleyebilir ve fagositler de bu tür ölen hücreyi etkili bir şekilde yutar .
Ancak ölen kanser hücreleri her zaman sessizce gitmez. Çalışmalar, ölmekte olan kanser hücrelerinin iltihaplanmayı tetikleyen kalıntıları serbest bırakarak bazen hayatta kalan kanser hücrelerinin büyümesini teşvik edebildiğini göstermektedir.
Révész etkisi olarak bilinen bu fenomen , bazı kanserlerin tedaviden sonra nasıl geri geldiğini açıklamaya yardımcı olabilir. İlk kez 1950’li yıllarda tümörlü farelerde gözlendi. Daha yakın zamanda, fareler ve laboratuvar kaplarındaki hücreler üzerinde 2018 yılında yapılan bir araştırma , radyasyon ve kemoterapinin , bazen tümör büyümesini destekleyebilen iltihabı tetikleyen, bağışıklık hücreleri tarafından salınan proinflamatuar sitokinlerin salınımını tetikleyebileceğini buldu .
L. RÉVÉSZ & NATURE Genetic Studies of the Relationship of Tumour–Host Cells: Effect of Tumour Cells killed by X-rays upon the Growth of Admixed Viable Cells
Boston’daki Beth Israel Deaconess Tıp Merkezi’nde çalışmanın ortak yazarı ve patoloji alanında yardımcı doçent olan Dr. Dipak Panigrahy , bir tür fagosit olan makrofajların kanserle savaşmak amacıyla bu molekülleri serbest bıraktığını söyledi .
tamamı için kaynağa bknz
ileri okuma:
CELL / Autoimmunity and the Clearance of Dead Cells
görsel ve ileri okuma